功能主治:适用于治疗轻度至重度高血压和心绞痛;静注能治疗高血压危象。适用于:1.轻、中度高血压病。2.高血压孕妇或先兆子痫。3.嗜铬细胞瘤。4.急进型高血压和高血压危象。5.控制全身麻醉时的低血压。
查看说明书药品对比
| 药品信息 | |||
| 主要成分 |
主要成分:盐酸拉贝洛尔。 |
化学名称为:2-[4-(4-氯苯甲酰基)苯氧基]–2-甲基-丙酸甲基乙酯 |
|
| 生产企业 |
大连美罗大药厂 |
RECIPHARM FONTAINE |
|
| 批准文号 |
国药准字H21023710 |
注册证号H20181239 |
|
| 说明 | |||
| 作用与功效 |
适用于治疗轻度至重度高血压和心绞痛;静注能治疗高血压危象。适用于:1.轻、中度高血压病。2.高血压孕妇或先兆子痫。3.嗜铬细胞瘤。4.急进型高血压和高血压危象。5.控制全身麻醉时的低血压。 |
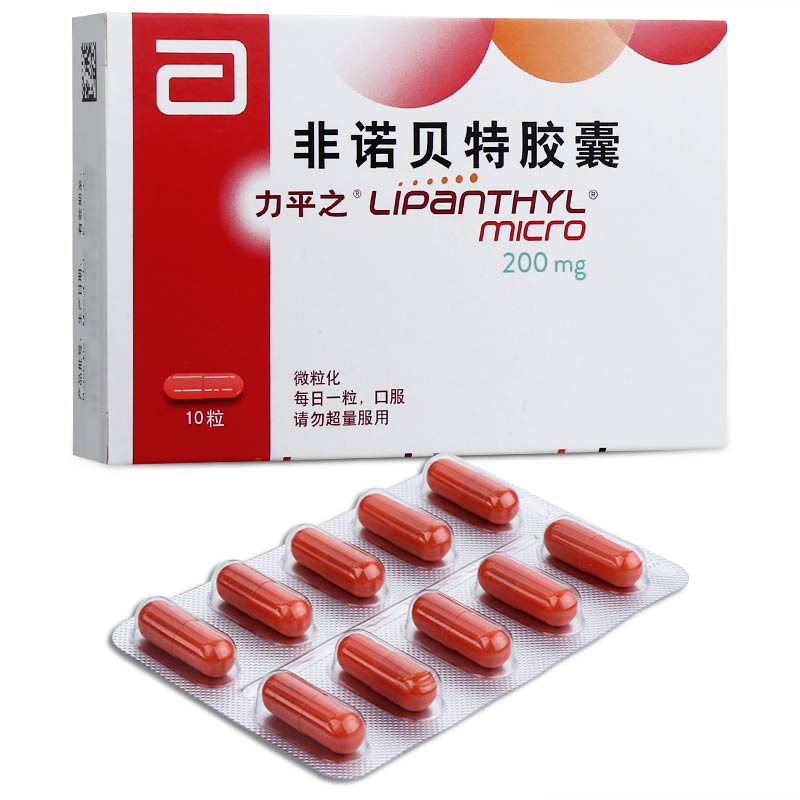
供成人使用:用于治疗成人饮食控制疗法效果不理想的高胆固醇血症(IIa型),内源性高甘油三酯血症,单纯型(IV型)和混合型(IIb和III型)。特别是饮食控制后血中胆固醇仍持续升高,或是有其他并发的危险因素时。在服药过程中应继续控制饮食。目前,尚无长期临床对照研究证明非诺贝特在动脉粥样硬化并发症一级和二级预防方面的有效性。尚未证明非诺贝特能够降低2型糖尿病患者的冠心病发病率和死亡。 |
|
| 用法用量 |
口服,常用量每次100~200mg,每日2~3次,于饭后服用。严重高血压时剂量可增至每次400mg,每日3~4次。每日剂量不超过2400mg。 |
配合饮食控制,该药可长期服用,并应定期监测疗效。每日服用一粒,与餐同服。当胆固醇的水平正常时,建议减少剂量。肾功能受损患者:轻中度肾功能受损患者建议从较小的起始剂量开始使用,然后根据对肾功能和血脂的影响,进行剂量调整。 |
|
| 副作用 |
脑溢血、心动过缓、传导阻滞及支气管哮喘患者。 |
因为不同对照临床试验之间的条件差别很大,因此不同临床试验的不良反应发生率难以直接进行比较,不一定能够代表实际使用中的发生率。以下为安慰剂对照双盲试验中,非诺贝特组发生率高于安慰剂组并且大于2%的不良事件列表,不论其因果关系如何。有大约5.0%的接受非诺贝特的患者、大约3%接受安慰剂的患者因为不良事件而停药。在双盲临床试验中,非诺贝特组最常见的导致停药的不良事件是肝功能检测异常,发生率是1.6%。(详见说明书表格)上市后经验:在上市后使用中自发报告了下列不良事件:肌痛、横纹肌溶解、胰腺炎、急性肾衰、肌痉挛、肝炎、肝硬化、贫血、关节痛、血红蛋白和红细胞压积降低、白细胞降低、哮喘。因为这些不良事件来自规模不确定的人群的自发报告,不一定能够对发生率进行准确的估计,也不一定能够确定是否与药物暴露有因果关系。 |
|
| 禁忌 |
|
孕妇及哺乳期妇女用药:孕期-动物试验结果显示未见有致畸作用。-到目前为至,临床尚未出现致畸和胚胎毒性。但对孕期使用非诺贝特的跟踪不足以排除任何危险,故一般孕妇应禁用。-贝特类药物不用于孕妇,但通过饮食控制不能有效降低高甘油三酯(>10g/L)而增加母体患急性胰腺炎危险的情况时除外。哺乳期目前尚无非诺贝特可进入母乳的资料。但在哺乳期禁用。儿童用药:尚未建立非诺贝特在儿童的安全性和有效性。老年用药:老年人的剂量选择取决于肾功能状态。肾功能正常的老年人通常不需要调整剂量。如有肾功能受损可以减少剂量。使用非诺贝特的老年患者可以进行肾功能的监测。 |
|
| 成分 |
适用于治疗轻度至重度高血压和心绞痛;静注能治疗高血压危象。适用于:1.轻、中度高血压病。2.高血压孕妇或先兆子痫。3.嗜铬细胞瘤。4.急进型高血压和高血压危象。5.控制全身麻醉时的低血压。 |
供成人使用:用于治疗成人饮食控制疗法效果不理想的高胆固醇血症(IIa型),内源性高甘油三酯血症,单纯型(IV型)和混合型(IIb和III型)。特别是饮食控制后血中胆固醇仍持续升高,或是有其他并发的危险因素时。在服药过程中应继续控制饮食。目前,尚无长期临床对照研究证明非诺贝特在动脉粥样硬化并发症一级和二级预防方面的有效性。尚未证明非诺贝特能够降低2型糖尿病患者的冠心病发病率和死亡。 |
|
| 药理作用 |
兼具α和β受体阻断作用的药物。有较弱的内在活性及膜稳定作用。阻断β受体的作用为阻断α受体作用的4-8倍;阻断β1受体的作用为普萘洛尔的1/4,阻断β2受体的作用为普萘洛尔的1/17-1/11。本品阻断β1受体的作用比阻断β2受体的作用比阻断β1受体作用略强。在等效剂量下,其心率减慢作用比普萘洛尔轻,降压作用出现较快。本品阻断α受体所致的血管舒张作用也参与降压和抗心绞痛机制。与单纯的β受体阻断药相比,该药在立位和运动试验时的降压作用较强。此外可使肾血流量增加,而普萘洛尔使之减少。 |
||
| 注意事项 |
心脏及肝、肾功能不全者慎用。给药期间患者应保持仰卧位,用药后要平卧3hr,以防体位性低血压发生。 |
|
|